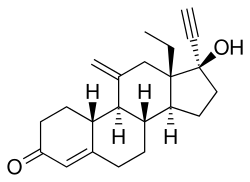
依托孕烯
 | |
 | |
| 臨床資料 | |
|---|---|
| 商品名 | Circlet、Implanon、Nexplanon及其他 |
| 其他名稱 | ORG-3236; SCH-900702 (with EE); 3-Ketodesogestrel; 3-Oxodesogestrel; 11-Methylenelevonorgestrel;[1] 11-Methylene-17α-ethynyl-18-methyl-19-nortestosterone; 11-Methylene-17α-ethynyl-18-methylestr-4-en-17β-ol-3-one |
| AHFS/Drugs.com | 专业药物信息 |
| MedlinePlus | a604032 |
| 懷孕分級 |
|
| 给药途径 | 皮下植入器、陰道避孕環 |
| 藥物類別 | 黃體酯酮 (藥物); 黃體素 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 |
|
| 藥物動力學數據 | |
| 生物利用度 | 植入:100%[4] 陰道避孕環:100%[5] |
| 血漿蛋白結合率 | ≥98%(66%與白蛋白,32%與性激素結合球蛋白)結合[4] |
| 药物代谢 | 肝臟(CYP3A4)[4][5] |
| 生物半衰期 | 21–38小時[6][7][8][4][5] |
| 排泄途徑 | 尿(主要)、糞便(少量)[4][5] |
| 识别信息 | |
| |
| CAS号 | 54048-10-1 |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.053.561 |
| 化学信息 | |
| 化学式 | C22H28O2 |
| 摩尔质量 | 324.46 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
| 依託孕烯節育植入裝置 | |
|---|---|
 植入裝置 | |
| 背景 | |
| 生育控制種類 | 單純孕酮避孕法 |
| 初次使用日期 | 1998 |
| 失敗率比率 (第一年) | |
| 完美使用 | 0.05% |
| 一般使用 | 0.05% |
| 用法 | |
| 持續期間 | 3 - 5年[9][10] |
| 可逆性 | 可逆 |
| 注意事項 | 3 -5年後需移除[11] |
| 優點及缺點 | |
| 是否可以防止性傳播疾病 | 否 |
| 是否影響體重 | 可能導致體重增加 |
| 月經 | 會導致月經不規則或延長經血時間 |
| 月經 | 少有經痛,33%的使用者沒有月經。 |
| 好處 | 長期避孕法 |
伊託孕烯(INN:etonogestrel)是一種商品名稱為Nexplanon和Implanon的裝置,供女性作避孕之用。[4][5][12][13]它以植入劑的形式提供,透過手術植入使用者上手臂皮膚之下。伊託孕烯是一種黃體酯酮 (藥物),也可與雌激素炔雌醇結合,作為商品名稱為NuvaRing和Circlet的陰道避孕環中使用。[14]伊託孕烯是一種非常有效的避孕方式,效果至少可持續3到4年,一些數據顯示其效果甚至可持續5年。[9][11]女性於裝置取出後可迅速恢復生育能力。[15]
使用伊託孕烯的副作用有月經不規律、乳房脹痛、情緒變化、痤瘡、頭痛、陰道炎等。[4]伊託孕烯是一種黃體酯酮,因此是孕酮受體的促效劑,而孕酮受體是黃體酯酮等黃體素的生物作用靶點。[4]它的作用機制是阻止排卵、增稠子宮頸開口黏液,以及改變子宮內膜。[16]此藥物具有非常微弱的雄激素和糖皮質激素活性,沒其他重要的激素活性。[17]
伊託孕烯於1972年取得專利,並於1998年開始用於醫療用途。[18][19][20]它於2006年獲准在美國上市。[18][19]截至2010年,伊託孕烯植入劑已在超過90個國家獲得批准,全球約有3百萬女性使用。[16][21]
一種密切相關且更廣為人知和使用的黃體酯酮 - 去氧孕烯,在使用者體內會代謝為伊託孕烯。[17]
醫療用途
[编辑]依託孕烯以避孕植入劑,[4]和避孕陰道環(與炔雌醇合併使用)劑的形式進行激素避孕。[5]
依託孕烯避孕植入劑是一種長效且可逆避孕法,已被證明是最有效的避孕方法之一。[22]由於此法在植入後不需使用者採取任何行動,因此無論是完美使用(完全遵照指示正確使用)還是典型使用(實際生活中,一般人使用避孕法的方式),植入劑的失敗率均為0.05%。[23]有項對此植入劑中的一種型號進行過研究,涉及超過2,467個婦女年的曝露,並沒發現有任何懷孕案例。[24][25][26]
其他研究則發現這種避孕法曾出現一些失敗案例,部分歸因於方法本身失效,部分歸因於植入不當、藥物交互作用或在植入前就已受孕。[27]
相比之下,輸卵管結紮的失敗率為0.5%,宮內節育器 (IUDs) 的失敗率為0.2–0.8%。[23]單個植入劑的批准使用期限為3年,但數據顯示其有效性可達5年。[28][11]
禁忌症
[编辑]女性在以下情況不應使用依託孕烯植入劑:[29]
- 懷孕或是認為自己可能懷孕
- 對依託孕烯過敏
- 有原因不明的陰道出血
- 患有某些形式的嚴重肝臟疾患
患有先兆偏頭痛的女性不應使用複合激素避孕藥 (簡稱CHC,例如前述陰道避孕環所含的藥物)。[30]
完整的禁忌症列表可在世界衛生組織(WHO)《避孕藥具使用醫療資格標準 2015(Medical Eligibility Criteria for Contraceptive Use 2015)》和美國疾病控制與預防中心(CDC)《美國避孕藥具使用醫療資格標準 2016(United States Medical Eligibility Criteria for Contraceptive Use 2016)》中找到。
副作用
[编辑]- 不規則出血和點滴出血。[31][24][25][26]
- 植入併發症。[24][24][32][27]
- 植入裝置移動。[32][24][33]
- 可能體重增加。[24][25]
- 卵巢囊腫。[24][34]
- 懷孕。[24]
- 痤瘡。[25]
- 其他可能症狀:曾報告過的其他症狀包括頭痛、情緒不穩、憂鬱、腹痛、性慾降低和陰道乾澀。[24]然而並無研究能明確判定這些症狀是由植入劑所引起。[25][26]
過量
[编辑]一般而言,過量服用此避孕藥將不會產生嚴重副作用。[35]
交互作用
[编辑]依非韋倫是一種肝酶CYP3A4的誘導劑,它可能與依託孕烯發生藥物交互作用,導致體內的依託孕烯濃度降低,[36]而升高藥物使用者發生意外懷孕風險。
其他CYP3A4誘導劑也可能產生類似交互作用,但其臨床重要性尚未被充分了解。反過來,CYP3A4抑制劑,例如酮康唑、伊曲康唑和克拉黴素,可能會抑制依託孕烯的代謝,而提高其在使用者體內的濃度。[35]
裝置描述
[编辑]
Nexplanon和Implanon是皮下植入的單一棒狀避孕器,由乙烯/醋酸乙烯酯共聚物製成,尺寸約為4公分長、2公釐直徑,[31]類似火柴棒。棒體內含68毫克的依託孕烯,[24]能持續釋放藥物。研究指出,植入初期血清中依託孕烯濃度會達到高峰(781–894皮克/毫升),之後緩慢下降,但3年後仍能維持在156–177皮克/毫升的穩定水平,確保使用者排卵受到抑制,達到避孕效果。[37]血清藥物濃度在36個月內呈現相對穩定,表示其避孕效力可能會長過3年。[38]
即使製造商官方批准的使用期限為3年,已有研究證明其高效避孕效果可維持長達5年。[28]
這是一種單純孕酮避孕法。
植入和取出
[编辑]植入物的手術須由經驗豐富的臨床醫師執行,以確保正確植入,並將神經損傷或錯位的風險降至最低,以避免因而懷孕。[39]
移除植入物時,會在其遠端區域再次進行局部麻醉。[24]若醫療人員無法透過觸覺檢測到植入物,則可能需要影像學檢查來確定植入桿的位置,然後在植入部位末端的皮膚上做一個小切口,再進行取出。某些情況下,植入物外可能已形成纖維鞘,此時就必須將此鞘切開。[24]接著會使用鑷子將植入物取出。平均來說,移除手術時間約為3至3.5分鐘。[25][26]
植入物移除後的生育力
[编辑]植入物移除後約一週,裝置釋放的激素會從使用者體內清除,大多數將不會再檢測到依托孕烯。[24]大多數女性會在移除後的6週內開始恢復排卵週期,[38][40]其生育力會恢復至植入前的水平。[15]
不同裝置間的差異
[编辑]Nexplanon和Implanon NXT兩種裝置與較早推出的Implanon本質上相同,主要的差別在於前兩者核心中額外添加有15毫克的硫酸鋇,因此能透過X光偵測到。[41][28]此外,Nexplanon和Implanon NXT還配備預裝填的植入器,讓植入手術更為簡便。 [42]
藥理學
[编辑]單純孕酮避孕法的作用機制取決於孕酮的活性和劑量。[43]中等劑量的單純孕酮避孕藥,如Nexplanon/Implanon,允許部分卵泡發育,但幾乎在所有週期中都能抑制排卵,成為其主要的作用機制。
此藥物的次要作用機制是會增加子宮頸黏液的黏稠度,而抑制精子穿透。[44]
此藥物也會對子宮內膜產生影響,理論上可影響受精卵著床,然而並無科學證據顯示它們可實際上阻止受精卵著床。[45]
藥效動力學
[编辑]依托孕烯是一種黃體酯酮,或稱孕酮受體促效劑。[17]相較於左炔諾孕酮和炔諾酮,它的雄性化作用較弱,[46][47]且不會降低性激素結合球蛋白的濃度。[48]
歷史
[编辑]於1940年代,由於可與人體相容的矽膠出現,而激發醫界開發皮下避孕植入劑的構想。[49]在1964年,研究證實此類植入棒可用於傳輸藥物。[50]在1966年,研究指出其釋放速率適合避孕。[51]總部設於美國紐約市的非營利組織 - 人口委員會(Population Council )後續開發並將六棒的Norplant及雙棒的Jadelle等植入劑裝置取得專利。[52]單棒植入劑裝置的開發是為解決Norplant六棒系統導致的的併發症,且單棒植入劑體積較小,植入後在皮膚外觀上較不明顯,並改充填依托孕烯以期減少副作用。[53][49]
依托孕烯的前體藥物去氧孕烯於1981年開始用於醫療用途。[6][7]Norplant自1983年起開始進入國際市場,於1993年進入美國和英國市場,但因移除的併發症多,於2002年在美國下架。雙棒的Jadelle雖獲美國食品藥物管理局(FDA)批准,卻未在美國銷售,而是在非洲和亞洲受廣泛使用。[52]
依托孕烯本身於1998年首次以Implanon名稱在印尼上市,[18][19]隨後在英國銷售,[54]並於2006年取得美國批准。[18][19]為解決Implanon的植入和定位問題,而開發Nexplanon,改良植入器,並讓植入棒具放射線顯影性。[41]Implanon自2012年1月起已停售,Nexplanon成為唯一的單棒植入劑裝置。
社會與文化
[编辑]Etonogestrel(依托孕烯)是此藥物的通用名稱,以及它的國際非專有藥名(INN)、美國採用名稱(USAN)和英國批准名稱(BAN)。[12][14]它也以其開發代碼名稱ORG-3236而聞名。[12][14]
品牌名稱
[编辑]依托孕烯以Circlet、Implanon、Nexplanon和NuvaRing等商品名稱於市面上銷售。[12][14]
供應
[编辑]依托孕烯在全球廣泛供應,包括美國、加拿大、英國、愛爾蘭、歐洲其他地區、南非、拉丁美洲、南亞、東亞和東南亞,以及世界其他地區。[14]
研究
[编辑]一種釋放依托孕烯的子宮內避孕系統曾被開發以供女性避孕用途,但開發工作已於2015年停止。[55]
依托孕烯也曾被研究作為潛在的男性避孕藥。[56]
參見
[编辑]參考文獻
[编辑]- ^ Ryan KJ. Kistner's Gynecology and Women's Health. Mosby. 1999: 300. ISBN 978-0-323-00201-1.
- ^ NEXPLANON : Etonogestrel extended release subdermal implant (PDF). Pdf.hres.ca. [2022-06-08]. (原始内容存档 (PDF)于2022-06-10).
- ^ List of nationally authorised medicinal products : Active substance: etonogestrel : Procedure no.: PSUSA/00001331/202109 (PDF). Ema.europa.eu. [2022-06-08]. (原始内容存档 (PDF)于2022-06-10).
- ^ 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 4.8 Nexplanon- etonogestrel implant. DailyMed. 2019-11-18 [2020-09-25]. (原始内容存档于2022-06-10).
- ^ 5.0 5.1 5.2 5.3 5.4 5.5 NuvaRing- etonogestrel and ethinyl estradiol insert, extended release. DailyMed. 2020-01-24 [2020-09-25]. (原始内容存档于2020-08-08).
- ^ 6.0 6.1 Runnebaum BC, Rabe T, Kiesel L. Female Contraception: Update and Trends. Springer Science & Business Media. 2012-12-06: 156–163. ISBN 978-3-642-73790-9.
- ^ 7.0 7.1 Holtsclaw JA. Progress Towards the Total Synthesis of Desogestrel and the Development of a New Chiral Dihydroimidazol-2-ylidene Ligand. University of Michigan. 2007: 25.
In 1981, desogestrel was marketed as a new low dose oral contraceptive under the trade names Marvelon and Desogen.32
- ^ Mosby's GenRx: A Comprehensive Reference for Generic and Brand Prescription Drugs. Mosby. 2001: 687. ISBN 978-0-323-00629-3.
The elimination half-life for 3-keto-desogestrel is approximately 38 ± 20 hours at steady state.
- ^ 9.0 9.1 Hamilton RJ. Tarascon Pocket Pharmacopoeia 2016 Deluxe Lab-Coat Edition. Jones & Bartlett Publishers. 2016: 392 [2021-02-18]. ISBN 9781284095289. (原始内容存档于2022-06-10).
- ^ Melville C. Sexual and Reproductive Health at a Glance. John Wiley & Sons. 2015: 21 [2021-02-18]. ISBN 9781118460757. (原始内容存档于2022-06-10).
- ^ 11.0 11.1 11.2 Lotke PS. Contraception, An Issue of Obstetrics and Gynecology Clinics, E-Book. Elsevier Health Sciences. 2016: 634 [2021-02-18]. ISBN 9780323402590. (原始内容存档于2022-05-09) (英语).
- ^ 12.0 12.1 12.2 12.3 Index Nominum 2000: International Drug Directory. Taylor & Francis. January 2000: 420 [2018-02-21]. ISBN 978-3-88763-075-1. (原始内容存档于2020-01-03).
- ^ Lemke TL, Williams DA. Foye's Principles of Medicinal Chemistry. Lippincott Williams & Wilkins. 2012-01-24: 1409– [2016-10-11]. ISBN 978-1-60913-345-0. (原始内容存档于2022-05-09).
- ^ 14.0 14.1 14.2 14.3 14.4 Etonogestrel. Drugs.com. [2017-08-03]. (原始内容存档于2017-08-03).
- ^ 15.0 15.1 World Health Organization. The selection and use of essential medicines. Twentieth report of the WHO Expert Committee 2015 (including 19th WHO Model List of Essential Medicines and 5th WHO Model List of Essential Medicines for Children). Geneva: World Health Organization. 2015: 332–36. ISBN 9789241209946. ISSN 0512-3054. hdl:10665/189763
 . WHO technical report series;994.
. WHO technical report series;994.
- ^ 16.0 16.1 Pattman R, Sankar N, Elawad B, Handy P, Price DA (编). Oxford Handbook of Genitourinary Medicine, HIV, and Sexual Health. OUP Oxford. 2010: 368. ISBN 9780199571666. (原始内容存档于2017-09-24).
- ^ 17.0 17.1 17.2 Kuhl H. Pharmacology of estrogens and progestogens: influence of different routes of administration (PDF). Climacteric. 2005, 8 (Suppl 1): 3–63 [2018-02-21]. PMID 16112947. S2CID 24616324. doi:10.1080/13697130500148875. (原始内容存档 (PDF)于2016-08-22).
- ^ 18.0 18.1 18.2 18.3 Carcio H, Secor RM. Advanced Health Assessment of Women, Third Edition: Clinical Skills and Procedures. Springer Publishing Company. 2014-10-10: 411– [2016-10-11]. ISBN 978-0-8261-2308-4. (原始内容存档于2022-05-09).
- ^ 19.0 19.1 19.2 19.3 Mayeaux EJ. The Essential Guide to Primary Care Procedures. Lippincott Williams & Wilkins. 2012-03-28: 589– [2016-10-11]. ISBN 978-1-4511-5286-9. (原始内容存档于2022-05-09).
- ^ Fischer J, Ganellin CR. Analogue-based Drug Discovery. John Wiley & Sons. 2006: 480 [2020-06-06]. ISBN 9783527607495. (原始内容存档于2022-05-09) (英语).
- ^ Senanayake P, Potts M. Atlas of Contraception, Second Edition 2. CRC Press. 2008: 53. ISBN 9780203347324. (原始内容存档于2017-09-24).
- ^ Winner B, Peipert JF, Zhao Q, Buckel C, Madden T, Allsworth JE, Secura GM. Effectiveness of long-acting reversible contraception. The New England Journal of Medicine. May 2012, 366 (21): 1998–2007 [2021-02-18]. PMID 22621627. S2CID 16812353. doi:10.1056/nejmoa1110855
 . (原始内容存档于2020-06-11).
. (原始内容存档于2020-06-11).
- ^ 23.0 23.1 Guttmacher. Contraceptive Use in the United States. 2012. (原始内容存档于2016-12-11).
- ^ 24.00 24.01 24.02 24.03 24.04 24.05 24.06 24.07 24.08 24.09 24.10 24.11 24.12 Raymond EG. Contraceptive Implants. Hatcher RA, Nelson TJ, Guest F, Kowal D (编). Contraceptive technology 19th revised. New York: Ardent Media. 2011: 144–156.
- ^ 25.0 25.1 25.2 25.3 25.4 25.5 Funk S, Miller MM, Mishell DR, Archer DF, Poindexter A, Schmidt J, Zampaglione E. Safety and efficacy of Implanon, a single-rod implantable contraceptive containing etonogestrel. Contraception. May 2005, 71 (5): 319–26. PMID 15854630. doi:10.1016/j.contraception.2004.11.007.
- ^ 26.0 26.1 26.2 26.3 Flores JB, Balderas ML, Bonilla MC, Vázquez-Estrada L. Clinical experience and acceptability of the etonogestrel subdermal contraceptive implant. International Journal of Gynaecology and Obstetrics. September 2005, 90 (3): 228–33. PMID 16043175. S2CID 2747597. doi:10.1016/j.ijgo.2005.06.007.
- ^ 27.0 27.1 Harrison-Woolrych M, Hill R. Unintended pregnancies with the etonogestrel implant (Implanon): a case series from postmarketing experience in Australia. Contraception. April 2005, 71 (4): 306–8. PMID 15792651. doi:10.1016/j.contraception.2004.10.005.
- ^ 28.0 28.1 28.2 Hatcher RA. Contraceptive technology. Hatcher, Robert A. (Robert Anthony), 1937- 21st. New York, NY. September 2018: Chapter 4, specifically pages 129–134. ISBN 978-1732055605. OCLC 1048947218.
- ^ US CDC Medical Eligibility Criteria for Contraceptive Use. 2016 [2021-02-18]. (原始内容存档于2019-06-21).
- ^ Nappi RE, Merki-Feld GS, Terreno E, Pellegrinelli A, Viana M. Hormonal contraception in women with migraine: is progestogen-only contraception a better choice?. The Journal of Headache and Pain. August 2013, 14 (1): 66. PMC 3735427
 . PMID 24456509. doi:10.1186/1129-2377-14-66
. PMID 24456509. doi:10.1186/1129-2377-14-66  .
.
- ^ 31.0 31.1 Adams K, Beal MW. Implanon: a review of the literature with recommendations for clinical management. Journal of Midwifery & Women's Health. 2009, 54 (2): 142–9. PMID 19249660. doi:10.1016/j.jmwh.2008.09.004
 .
.
- ^ 32.0 32.1 Smith A, Reuter S. An assessment of the use of Implanon in three community services. The Journal of Family Planning and Reproductive Health Care. October 2002, 28 (4): 193–6. PMID 12419059. doi:10.1783/147118902101196540
 .
.
- ^ Nexplanon (etonogestrel) contraceptive implants: Reports of device in vasculature and lung. [2016-07-31]. (原始内容存档于2016-09-18).
- ^ Brache V, Faundes A, Alvarez F, Cochon L. Nonmenstrual adverse events during use of implantable contraceptives for women: data from clinical trials. Contraception. January 2002, 65 (1): 63–74. PMID 11861056. doi:10.1016/s0010-7824(01)00289-x.
- ^ 35.0 35.1 Haberfeld H (编). Austria-Codex. Vienna: Österreichischer Apothekerverlag. 2020. Implanon NXT 68 mg Implantat zur subkutanen Anwendung (German).
- ^ Vieira CS, Bahamondes MV, de Souza RM, Brito MB, Rocha Prandini TR, Amaral E, et al. Effect of antiretroviral therapy including lopinavir/ritonavir or efavirenz on etonogestrel-releasing implant pharmacokinetics in HIV-positive women. Journal of Acquired Immune Deficiency Syndromes. August 2014, 66 (4): 378–385. PMID 24798768. S2CID 19545105. doi:10.1097/QAI.0000000000000189
 .
.
- ^ Implanon label (PDF). FDA. 2010-10-26 [2010-10-26]. (原始内容存档于2010-03-10).
- ^ 38.0 38.1 Mäkäräinen L, van Beek A, Tuomivaara L, Asplund B, Coelingh Bennink H. Ovarian function during the use of a single contraceptive implant: Implanon compared with Norplant. Fertility and Sterility. April 1998, 69 (4): 714–21. PMID 9548163. doi:10.1016/s0015-0282(98)00015-6
 .
.
- ^ Wechselberger G, Wolfram D, Pülzl P, Soelder E, Schoeller T. Nerve injury caused by removal of an implantable hormonal contraceptive. American Journal of Obstetrics and Gynecology. July 2006, 195 (1): 323–6. PMID 16813761. doi:10.1016/j.ajog.2005.09.016.
- ^ Davies GC, Feng LX, Newton JR, Van Beek A, Coelingh-Bennink HJ. Release characteristics, ovarian activity and menstrual bleeding pattern with a single contraceptive implant releasing 3-ketodesogestrel. Contraception. March 1993, 47 (3): 251–61. PMID 8462316. doi:10.1016/0010-7824(93)90042-6.
- ^ 41.0 41.1 Mansour D. Nexplanon: what Implanon did next. The Journal of Family Planning and Reproductive Health Care. October 2010, 36 (4): 187–9. PMID 21067632. doi:10.1783/147118910793048629
 .
.
- ^ Ormsby A. Contraceptive alert after women fall pregnant. Reuters. 2011-01-05 [2011-05-10]. (原始内容存档于2012-05-22).
- ^ Glasier A. Contraception. DeGroot LJ, Jameson JL (编). Endocrinology 5th. Philadelphia: Elsevier Saunders. 2006: 3000–1. ISBN 978-0-7216-0376-6.
- ^ Organon. Implanon SPC (Summary of Product Characteristics). April 2006 [2007-04-15]. (原始内容存档于2007-09-30).
- ^ Rivera R, Yacobson I, Grimes D. The mechanism of action of hormonal contraceptives and intrauterine contraceptive devices. American Journal of Obstetrics and Gynecology. November 1999, 181 (5 Pt 1): 1263–9. PMID 10561657. doi:10.1016/S0002-9378(99)70120-1.
- ^ Danby FW. Acne: Causes and Practical Management. John Wiley & Sons. 27 January 2015: 77– [11 October 2016]. ISBN 978-1-118-23277-4. (原始内容存档于9 May 2022).
- ^ Golan DE. Principles of Pharmacology: The Pathophysiologic Basis of Drug Therapy. Lippincott Williams & Wilkins. 2008: 521– [2016-10-11]. ISBN 978-0-7817-8355-2. (原始内容存档于2022-05-09).
- ^ Speroff L, Darney PD. A Clinical Guide for Contraception. Lippincott Williams & Wilkins. 2010-11-22: 365– [2016-10-11]. ISBN 978-1-60831-610-6. (原始内容存档于2022-05-09).
- ^ 49.0 49.1 Ladipo OA, Akinso SA. Contraceptive implants. African Journal of Reproductive Health. April 2005, 9 (1): 16–23. JSTOR 3583156. PMID 16104651. doi:10.2307/3583156.
- ^ Folkman J, Long DM. The use of silicone rubber as a carrier for prolonged drug therapy. The Journal of Surgical Research. March 1964, 4 (3): 139–42. PMID 14130164. doi:10.1016/s0022-4804(64)80040-8.
- ^ Dziuk PJ, Cook B. Passage of steroids through silicone rubber. Endocrinology. January 1966, 78 (1): 208–11. PMID 5948426. doi:10.1210/endo-78-1-208.
- ^ 52.0 52.1 Association of Reproductive Health Professionals. The Single-Rod Contraceptive Implant. July 2008. (原始内容存档于2018-03-20).
- ^ US granted 4957119,De Nijs H,「Contraceptive Implant」,发行于18 September 1990,指定于Akzo NV
- ^ Glasier A, Winikoff B. Contraception. Health Press. December 1999: 41 [2016-10-11]. ISBN 978-1-899541-18-8. (原始内容存档于2022-05-09).
- ^ Etonogestrel-releasing intrauterine system - Merck & Co.. Adisinsight.springer.com. [2018-02-21]. (原始内容存档于2022-06-10).
- ^ Nieschlag E. Clinical trials in male hormonal contraception (PDF). Contraception. 2010, 82 (5): 457–70 [2020-09-05]. PMID 20933120. doi:10.1016/j.contraception.2010.03.020. (原始内容存档 (PDF)于2020-12-05).
延伸閱讀
[编辑]- Bennink HJ. The pharmacokinetics and pharmacodynamics of Implanon, a single-rod etonogestrel contraceptive implant. Eur J Contracept Reprod Health Care. September 2000, 5 (Suppl 2): 12–20. PMID 11246602. S2CID 67921250. doi:10.1080/14730782.2000.12288981.
- Varma R, Mascarenhas L. Endometrial effects of etonogestrel (Implanon) contraceptive implant. Curr. Opin. Obstet. Gynecol. June 2001, 13 (3): 335–41. PMID 11396660. S2CID 45520124. doi:10.1097/00001703-200106000-00015.
- Etonogestrel implant (Implanon) for contraception. Drug Ther Bull. August 2001, 39 (8): 57–9. PMID 11526801.
- Gaffield ME, Curtis KM, Mohllajee AP, Peterson HB. Medical eligibility criteria for new contraceptive methods: combined hormonal patch, combined hormonal vaginal ring and the etonogestrel implant. Contraception. February 2006, 73 (2): 134–44. PMID 16413844. doi:10.1016/j.contraception.2005.08.002.
- Wagner MS, Arias RD, Nucatola DL. The combined etonogestrel/ethinyl estradiol contraceptive vaginal ring. Expert Opin Pharmacother. August 2007, 8 (11): 1769–77. PMID 17685892. S2CID 42412888. doi:10.1517/14656566.8.11.1769.
- Mansour D, Bahamondes L, Critchley H, Darney P, Fraser IS. The management of unacceptable bleeding patterns in etonogestrel-releasing contraceptive implant users. Contraception. March 2011, 83 (3): 202–10. PMID 21310280. doi:10.1016/j.contraception.2010.08.001.
- In brief: etonogestrel (nexplanon) contraceptive implant. The Medical Letter on Drugs and Therapeutics. February 2012, 54 (1383): 12. PMID 22354222.
- Stuebe AM, Bryant AG, Lewis R, Muddana A. Association of Etonogestrel-Releasing Contraceptive Implant with Reduced Weight Gain in an Exclusively Breastfed Infant: Report and Literature Review. Breastfeed Med. May 2016, 11 (4): 203–6. PMC 4860664
 . PMID 27032034. doi:10.1089/bfm.2016.0017.
. PMID 27032034. doi:10.1089/bfm.2016.0017. - López-Picado A, Lapuente O, Lete I. Efficacy and side-effects profile of the ethinylestradiol and etonogestrel contraceptive vaginal ring: a systematic review and meta-analysis. Eur J Contracept Reprod Health Care. April 2017, 22 (2): 131–146. PMID 28256919. S2CID 24447820. doi:10.1080/13625187.2017.1287351.
外部連結
[编辑]
