三氟化溴
外观
| 三氟化溴 | |
|---|---|
| |
| |
| 识别 | |
| CAS号 | 7787-71-5 |
| PubChem | 24594 |
| ChemSpider | 22996 |
| SMILES |
|
| UN编号 | 1746 |
| 性质 | |
| 化学式 | BrF3 |
| 摩尔质量 | 136.90 g·mol⁻¹ |
| 外观 | 稻草色液体 吸湿性 |
| 密度 | 2.803 g/cm3 [1] |
| 熔点 | 8.77 °C |
| 沸点 | 125.72 °C |
| 溶解性(水) | 分解 |
| 溶解性(硫酸) | 可溶 |
| 结构 | |
| 分子构型 | T形(C2v) |
| 偶极矩 | 1.19 D |
| 危险性 | |
| 欧盟分类 | 未列出 |
| NFPA 704 | |
| 相关物质 | |
| 其他阴离子 | 一氯化溴 |
| 其他阳离子 | 三氟化氯 三氟化碘 |
| 相关化学品 | 一氟化溴 五氟化溴 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
三氟化溴是一种卤素互化物,化学式为BrF3。这种无色、有毒、有腐蚀性的液体可溶于硫酸,但与水或有机化合物接触会发生爆炸。它是一种强氟化剂和无机离子化溶剂。它在核燃料生产和后处理过程中被用于生产六氟化铀(UF6)。[2]
制备
[编辑]三氟化溴最早由保罗·利比奥(Paul Lebeau)于1906年报道。他将溴单质与氟在20 °C下反应得到了三氟化溴:[3]
结构
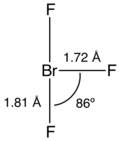
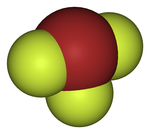
[编辑]与ClF3和IF3类似,BrF3分子也是T形的。价层电子对互斥理论中,中心溴原子连有两对孤对电子。每个轴向的Br-F键长度为1.81 Å,而水平方向的为1.72 Å。轴向Br-F键与水平Br-F键的夹角略小于90°,86.2°的键角是因为孤对电子的排斥比成键电子更强,键角的变小使得能量降低。[5][6]
化学性质
[编辑]BrF3是一种强氟化剂,但略弱于ClF3。这种液体能导电,因为它能发生自耦电离:[2]
许多离子型氟化物易溶于三氟化溴,并形成溶剂合碱(即路易斯酸碱的加合物):[2]
此外少数共价型氟化物,例如四氟化硅、五氟化钒及类似化合物也可溶于三氟化溴,它们在溶液中作为路易斯酸。
含BrF2+的物质与含BrF4-能发生类似于酸碱中和的反应:
这类反应被广泛用于制取含氟配合物,例如AgAuF4、(NO2)SnF6、(NO)2SnF6、LiVF6、KRuF6等,在上述反应完成后真空蒸发除去三氟化溴即可得到产品。
三氟化溴能使高价氟配合物稳定,例如四氟化钯不能分离得到,但在三氟化溴中可制得它的配合物。稀有气体的氟化物也能在三氟化溴中与强路易斯酸形成加合物。[7]
参考资料
[编辑]- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
- ^ 2.0 2.1 2.2 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Lebeau P. The effect of fluorine on chloride and on bromine. Annales de Chimie et de Physique. 1906, 9: 241–263.
- ^ Simons JH; Yost, Don M.; Rogers, M. T. Bromine (III) Fluoride - Bromine Trifluoride. Inorganic Synthesis. 1950, 3: 184–186. doi:10.1002/9780470132340.ch48.
- ^ Gutmann V. Die Chemie in Bromtrifuoride. Angewante Chemie. 1950, 62: 312–315. doi:10.1002/ange.19500621305.
- ^ Meinert H. Interhalogenverbindungen. Zeitschrift für Chemie. 1967, 7: 41.
- ^ 张青莲. 《无机化学丛书》第六卷:卤素、铜分族、锌分族. 北京: 科学出版社. : P412–414. ISBN 7-03-002238-6.








