氟化鉛
外觀
此條目需要補充更多來源。 (2022年12月13日) |
| 氟化鉛 | |
|---|---|

| |
| |
| 別名 | 二氟化鉛 |
| 識別 | |
| CAS號 | 7783-46-2 |
| PubChem | 24549 |
| 性質 | |
| 化學式 | PbF2 |
| 摩爾質量 | 245.20 g·mol⁻¹ |
| 外觀 | 白色粉末 |
| 氣味 | 無味 |
| 密度 | 8.445 g/cm3 (orthorhombic) 7.750 g/cm3 (cubic) |
| 熔點 | 824°C |
| 沸點 | 1293°C |
| 溶解性(水) | 0.057 g/100 mL (0 °C) 0.0671 g/100 mL (20 °C)[1] |
| 溶度積Ksp | 2.05 x 10-8 (20 °C) |
| 溶解性 | 可溶於硝酸中 不溶於丙酮及氨 |
| 結構 | |
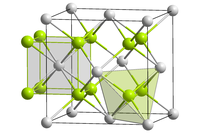
| 晶體結構 | 螢石(cubic),cF12 |
| 空間群 | Fm3m, No. 225 |
| 危險性 | |
| 致死量或濃度: | |
LD50(中位劑量)
|
3031 mg/kg(大鼠口服) |
| 相關物質 | |
| 其他陰離子 | 氯化鉛 溴化鉛 碘化鉛 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氟化鉛(Lead(II) fluoride)化學式為PbF2,是白色固體。氟化鉛有同質異形體,在常溫下為正交晶系(PbCl2型),在高溫下則是立方晶系(Fluorite type)[2]。
製備
[編輯]氟化鉛可以用多種方式製備,可以將氫氧化鉛或碳酸鉛和氫氟酸反應,再將生成物中的水蒸發而得[3]:
- Pb(OH)2 + 2 HF → PbF2 + 2 H2O
氟化鉛也可以用在鉛鹽溶液中加入氫氟酸,或是在硝酸鉛溶液中加入氟化鉀[4]:
- 2 KF + Pb(NO3)2 → PbF2 + 2 KNO3
- 2 NaF + Pb(CH3COO)2 → PbF2 + 2 NaCH3COO
用途
[編輯]氟化鉛可以用在低熔點的玻璃、可以反應紅外線的玻璃塗層、CRT電視的磷光體,以及製造甲基吡啶時的催化劑[3]。繆子g-2粒子物理實驗就是用PbF
2閃爍體探測器配合矽的光電倍增器[5]。
參考資料
[編輯]- ^ NIST-data review 1980
- ^ Haines, J.; Léger, J. M.; Schulte, O. High-pressure isosymmetric phase transition in orthorhombic lead fluoride. Physical Review B (American Physical Society (APS)). 1998-04-01, 57 (13): 7551–7555. Bibcode:1998PhRvB..57.7551H. ISSN 0163-1829. doi:10.1103/physrevb.57.7551.
- ^ 3.0 3.1 Carr, Dodd S., Lead Compounds, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a15_249
- ^ Arnold Hollemann, Egon Wiberg, 101st ed., de Gruyter 1995 Berlin; ISBN 3-11-012641-9
- ^ Grange, J.; et al. Muon (g−2) Technical Design Report. Jan 27, 2015. Bibcode:2015arXiv150106858G. arXiv:1501.06858
 . 已忽略未知參數
. 已忽略未知參數|collaboration=(幫助) Via inSPIRE (頁面存檔備份,存於互聯網檔案館)
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
